AGREGUE A SU WHATSSAP EL +51 962685431 Y PARTICIPE DE LOS CIENTOS DE GRUPOS DE ÓPTICOS , OPTOMETRAS , OFTALMOLOGOS Y EMPRESAS ÓPTICAS DE...
Toxicidad ocular medicamentosa ( Tamoxifeno. Hidroxicloroquina. Anticolinérgicos. Tamsulosina. Ifis.)
Author: Infolentes
Rating 5 of 5 Des:
AGREGUE A SU WHATSSAP EL +51 962685431 Y PARTICIPE DE LOS CIENTOS DE GRUPOS DE ÓPTICOS , OPTOMETRAS , OFTALMOLOGOS Y EMPRESAS ÓPTICAS DE...
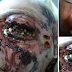
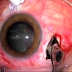
Mira: Quitando gusanos del ojo de la mujer
Author: Infolentes
Rating 5 of 5 Des:
AGREGUE A SU WHATSSAP EL +51 962685431 Y PARTICIPE DE LOS CIENTOS DE GRUPOS DE ÓPTICOS , OPTOMETRAS , OFTALMOLOGOS Y EMPRESAS ÓPTICAS DE...
Eliminación del quiste de párpado dermoide
Author: Infolentes
Rating 5 of 5 Des:
AGREGUE A SU WHATSSAP EL +51 962685431 Y PARTICIPE DE LOS CIENTOS DE GRUPOS DE ÓPTICOS , OPTOMETRAS , OFTALMOLOGOS Y EMPRESAS ÓPTICAS DE...
Quiste dentro del globo ocular
Author: Infolentes
Rating 5 of 5 Des:
AGREGUE A SU WHATSSAP EL +51 962685431 Y PARTICIPE DE LOS CIENTOS DE GRUPOS DE ÓPTICOS , OPTOMETRAS , OFTALMOLOGOS Y EMPRESAS ÓPTICAS DE...
Inervación parasimpática y simpática de los músculos iris.
Author: Infolentes
Rating 5 of 5 Des:
AGREGUE A SU WHATSSAP EL +51 962685431 Y PARTICIPE DE LOS CIENTOS DE GRUPOS DE ÓPTICOS , OPTOMETRAS , OFTALMOLOGOS Y EMPRESAS ÓPTICAS DE...
Peru . La OMS recomienda esta cantidad de azucar al dia . inclreible
Author: Infolentes
Rating 5 of 5 Des:
AGREGUE A SU WHATSSAP EL +51 962685431 Y PARTICIPE DE LOS CIENTOS DE GRUPOS DE ÓPTICOS , OPTOMETRAS , OFTALMOLOGOS Y EMPRESAS ÓPTICAS DE...
Ya es un hecho que PPK renunció a la presidencia del Perú
Author: Infolentes
Rating 5 of 5 Des:
AGREGUE A SU WHATSSAP EL +51 962685431 Y PARTICIPE DE LOS CIENTOS DE GRUPOS DE ÓPTICOS , OPTOMETRAS , OFTALMOLOGOS Y EMPRESAS ÓPTICAS DE...
Terapia génica para coroideremia
Author: Infolentes
Rating 5 of 5 Des:
AGREGUE A SU WHATSSAP EL +51 962685431 Y PARTICIPE DE LOS CIENTOS DE GRUPOS DE ÓPTICOS , OPTOMETRAS , OFTALMOLOGOS Y EMPRESAS ÓPTICAS DE...
Secuenciarán los genomas de 100 pacientes con una rara discapacidad visual
Author: Infolentes
Rating 5 of 5 Des:
AGREGUE A SU WHATSSAP EL +51 962685431 Y PARTICIPE DE LOS CIENTOS DE GRUPOS DE ÓPTICOS , OPTOMETRAS , OFTALMOLOGOS Y EMPRESAS ÓPTICAS DE...
Perú Google Flights, la herramienta para encontrar vuelos baratos
Author: Infolentes
Rating 5 of 5 Des:
AGREGUE A SU WHATSSAP EL +51 962685431 Y PARTICIPE DE LOS CIENTOS DE GRUPOS DE ÓPTICOS , OPTOMETRAS , OFTALMOLOGOS Y EMPRESAS ÓPTICAS DE...
En EE.UU. preocupante estudio revela terrible secreto del agua embotellada SE RECOMIENDA EL USO DE BOTELLAS DE
Author: Infolentes
Rating 5 of 5 Des:
AGREGUE A SU WHATSSAP EL +51 962685431 Y PARTICIPE DE LOS CIENTOS DE GRUPOS DE ÓPTICOS , OPTOMETRAS , OFTALMOLOGOS Y EMPRESAS ÓPTICAS DE...
Estudiantes del I ciclo Taller de Óptica Oftálmica. Prof. Reinhard Müller, Alemania 50 nuevos estudiantes. Nueva generación de Optometria
Author: Infolentes
Rating 5 of 5 Des:
AGREGUE A SU WHATSSAP EL +51 962685431 Y PARTICIPE DE LOS CIENTOS DE GRUPOS DE ÓPTICOS , OPTOMETRAS , OFTALMOLOGOS Y EMPRESAS ÓPTICAS DE...